糖尿病可以被治愈了!
近一年来,上海长征医院副院长殷浩团队取得了一系列突破性成果:去年5月,全球首次利用自体干细胞再生疗法成功治愈重度2型糖尿病患者;近期,又宣布通过干细胞再生移植疗法成功治愈了多位1型糖尿病患者。
目前,由殷浩团队联合开发的“异体人再生胰岛注射液”,已获得国家药监局临床试验默示许可,成为中国第一个,全球第二个进入临床试验阶段的异体通用型再生胰岛产品。这不仅是糖尿病治疗史的里程碑,更是全球干细胞疗法竞赛的转折点。
当传统治疗还在“控制病情”层面徘徊时,干细胞疗法已悄然叩开“治愈”的大门。更令人惊叹的是,这仅仅是干细胞治疗革命的冰山一角……
01
一场医学革命被引爆了
干细胞疗法治愈糖尿病取得重大突破,开启了一个颠覆传统治疗范式的新时代,也引爆了一场医学革命。
相比传统治疗模式,干细胞疗法究竟有何过人之处?
所谓干细胞,是具有强大的再生、自我复制和修复能力的多潜能细胞,在一定条件下,可以分化成多种功能细胞。
干细胞的分类复杂且多元化,呈现出显著的层级化特征:按发育阶段划分,可分为胚胎干细胞(nESC)、成体干细胞、诱导多功能干细胞(iPSC)三大类;按分化潜能划分,可分为全能干细胞,多能干细胞、单能干细胞。其中,多能干细胞又可划分为间充质干细胞(MSC)、造血干细胞。
这种多维度的分类框架,为干细胞技术在诸多重大疾病的治疗应用提供了理论基础。
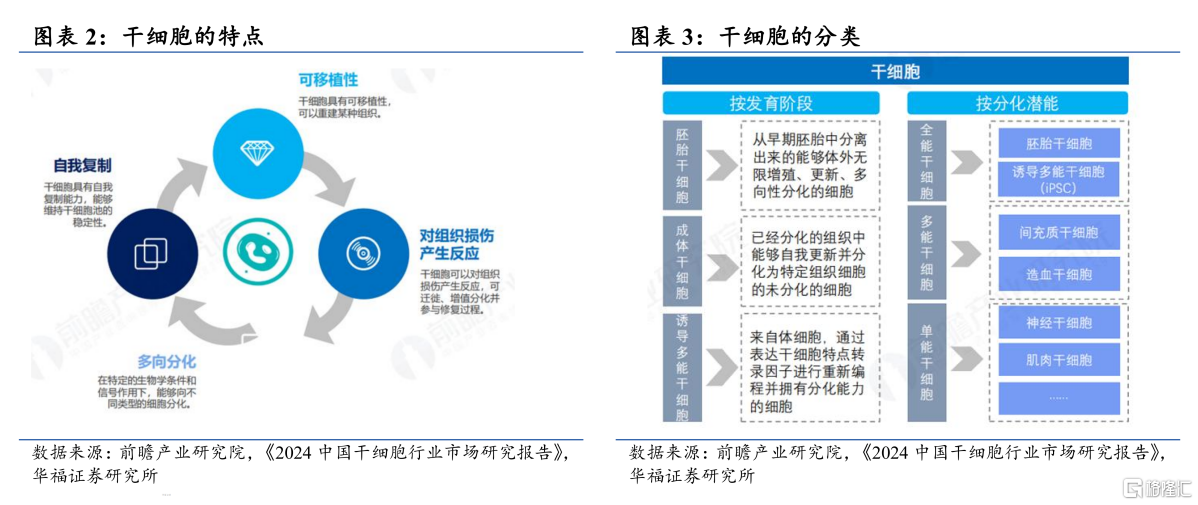
图片来源:华福证券研报
干细胞治疗是通过将健康的干细胞移植到患者的体内,修复和替代受损或死亡的细胞,以恢复机体的正常功能,未来可应用在多种重大疾病,而不仅仅用于治疗糖尿病。
根据ClinicalTrials.gov的数据,全球有超过7230项干细胞疗法的临床试验正在进行,涵盖几乎所有人体系统,尤其在传统疗法难以治疗的疾病中,干细胞疗法展现出了巨大的潜力。
以临床应用研究最多的间充质干细胞(MSCs)为例,目前已在多种疾病中发挥了良好的治疗作用,包括移植物抗宿主病、肾脏损伤、组织器官移植的免疫耐受、神经损伤、风湿性疾病、肝脏疾病等。
2024年,有多款MSC产品获批上市,确立了MSC成药的商业化通路:
7月,日本SanBio株式会社研发的“AKUUGO®颅内植入混悬液”(Vandefitemcel),在日本获得有条件上市批准,成为全球首个用于创伤性脑损伤(TBI)引起的慢性运动性瘫痪的同种异体细胞治疗药物;
12月,Mesoblast Limited研发的同种异体骨髓间充质基质细胞疗法Ryoncil(remestemcel-L-rknd)获FDA批准上市,用于治疗2个月及以上儿科患者的类固醇难治性急性移植物抗宿主病(SR-aGvHD),成为首个获FDA批准的MSC疗法。
从市场前景看,由于对再生医学和研究资助的需求增加,全球干细胞治疗市场正在以极快的速度增长。根据Dimension Market Research的数据,全球干细胞治疗市场规模将由2024年的189亿美元激增至2033年的547亿美元,2024-2033E的CAGR为12.6%。
02
干细胞疗法的黄金时代
干细胞疗法不再是停留在实验室阶段的概念产品,而是已经实现规模化商业应用,迎来了黄金时代。
根据相关文献统计,目前世界各地的监管机构批准的MSCs疗法共包含12项,其中韩国5款、欧盟2款、日本2款。其中,韩国Pharmicell公司研发的Cellgram,是全球首个获批的干细胞药物(2011年上市),用于治疗急性心肌梗死,2018年达到25亿韩元(约180万美元)的峰值。
由韩国另一家干细胞产业领军企业Medipost研发的Cartistem,是世界首个同种异体脐带血干细胞疗法(2012年上市),适应证为膝关节骨关节炎,累计销售额达1080亿韩元(约7809万美元),2023年超过200亿韩元(约1440万美元)。
尤其是,Ryoncil作为FDA首个批准上市的MSC疗法,未来市场表现值得期待。目前,急性移植物抗宿主病(aGVHD)一线治疗仍为糖皮质激素,最常应用甲泼尼龙,一线治疗有效率仅约50%。约一半患者为类固醇难治性aGVHD(SRaGVHD),后者远期生存率不足20%。而根据临床研究结果显示,Ryoncil的临床患者2年总体生存率达51%。
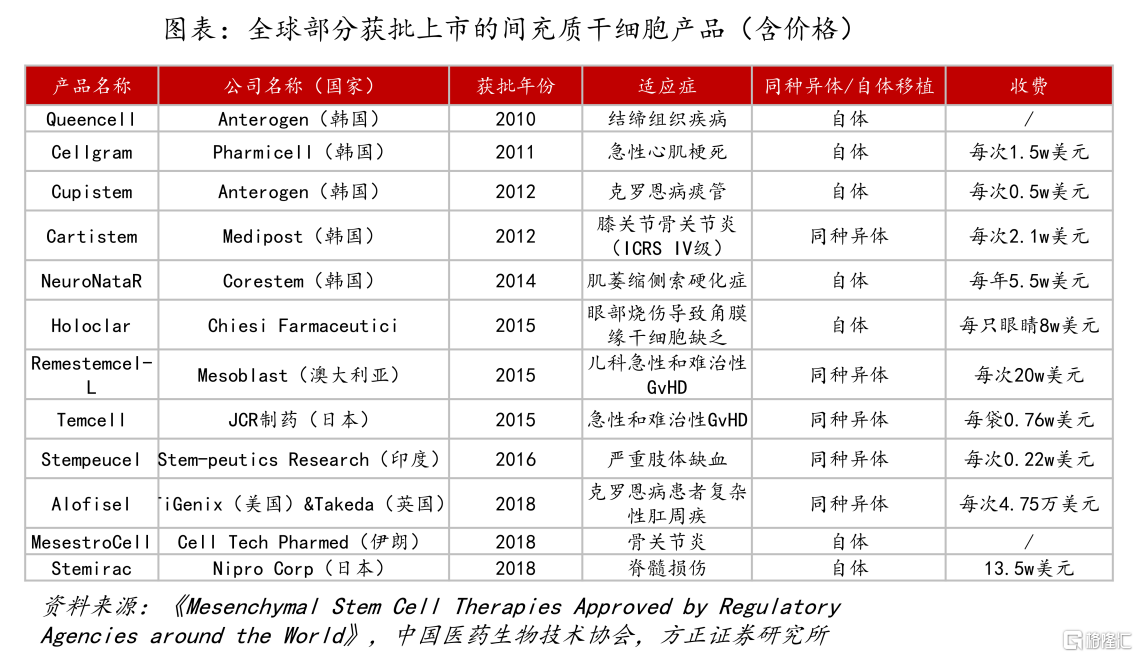
图片来源:方正证券研报
尽管当前全球已获批的干细胞疗法较少,但却呈现出快速发展态势。根据NextPharma®数据库的统计,截至2024年3月,全球干细胞疗法管线数量高达933个,其中有不少潜在重磅管线值得关注。
例如,福泰制药(Vertex)公司研发的VX-880,目前已进入Ⅲ期临床,有望成为全球首个针对特定1型糖尿病患者的干细胞疗法。VX-880在2021年名声大噪,彼时新闻报道其成功治愈了一名糖尿病病史长达40年且伴有严重反复低血糖反应的1型糖尿病重症患者。
Neurona Therapeutics的异体现货型细胞疗法NRTX-1001,将于2025年下半年启动用于关键性III期EPIC试验,是全球首个针对耐药性癫痫的再生细胞疗法。NRTX-1001源自人类多能干细胞,通过移植GABA能中间神经元,持久恢复大脑抑制性网络平衡,避免组织损伤风险。
此外,还有不少MNC巨头进军干细胞疗法领域。
拜耳通过收购BlueRock Therapeutics切入干细胞治疗赛道,后者专注于基于iPSC的细胞疗法,其用于治疗帕金森病的干细胞衍生疗法Bemdaneprocel(BRT-DA01)将于2025年上半年启动III期临床试验,有望成为首个针对神经退行性疾病的同种异体细胞疗法。
礼来以超3亿美元收购Sigilon,后者致力于针对广泛急性和慢性疾病开发功能性治愈疗法。双方曾在2018年达成研发合作,利用改良版的干细胞疗法开发1型糖尿病细胞疗法,这项合作涉及胰岛细胞封装技术。
诺和诺德以26亿美元总交易额与Aspect Biosystems达成合作,引进4款用于治疗糖尿病和肥胖症的生物打印组织疗法,这是基于诺和诺德在干细胞分化和细胞疗法开发与制造方面的积累。
03
中国药企的进击之路
在这场医疗革命的浪潮中,中国药企的身影尤为引人注目。根据NextPharma数据库的统计,截至2024年3月,全球干细胞疗法管线数量为933个,中国干细胞疗法管线数量为296个,全球管线占比达32%,位居第二。
另外,根据CDE网站数据的不完全统计,截至2024年12月底,CDE共受理间充质干细胞IND申请127项,其中98项获得默示许可,涉及自身免疫性疾病、呼吸系统、消化系统、骨关节病、神经系统等多种疾病。注册临床研究进展方面,5项进入III期临床试验,9项进入II期临床试验。
可见,我国干细胞治疗行业呈现出百花齐放、百家争鸣的盛况。尤其是今年,我国首款干细胞药品获批上市,实现了从0到1的突破。
2025年1月2日,NMPA附条件批准了铂生卓越研发的人脐带间充质干细胞新药艾米迈托赛注射液,用于治疗14岁以上消化道受累为主的激素治疗失败的急性移植物抗宿主病。根据泽辉生物招股书(申报稿)转引弗若斯特沙利文的资料,2024年中国全年约有1.1万例新发aGVHD。
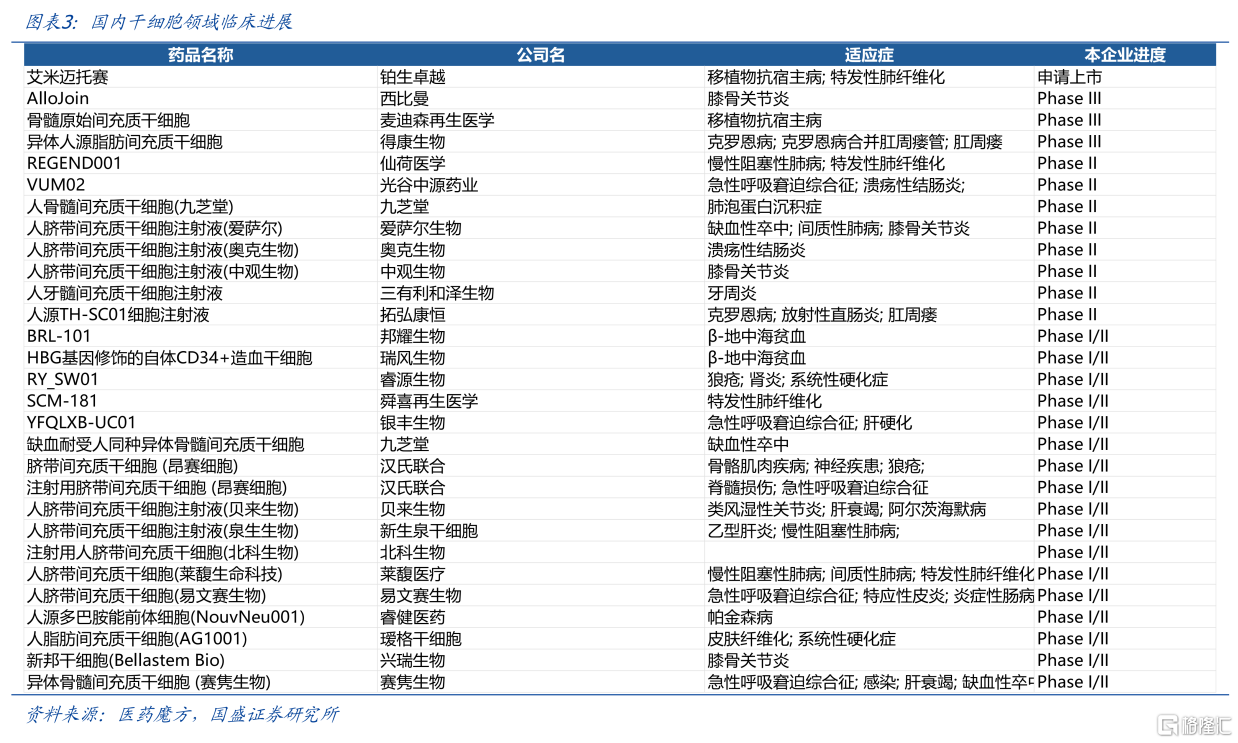
国内干细胞领域临床进展(数据截至2024年12月22日)
图片来源:国盛证券研报
在这一领域,我国已有多家上市公司,包括中源协和、冠昊生物、汉氏联合、顺昊生物、天晴股份。一级市场方面,2024年有多家干细胞药物研发公司获得融资,包括中盛溯源、睿健医药、士泽生物、瑞普晨创。
从研发管线看,中源协和布局了多个间充质干细胞药物,包括VUM02注射液(已有8个适应证获批临床)、脐带间充质干细胞(已有4个适应证获批临床);另外,其参股公司三有利和泽的人牙髓间充质干细胞,已有2个适应证获批临床。
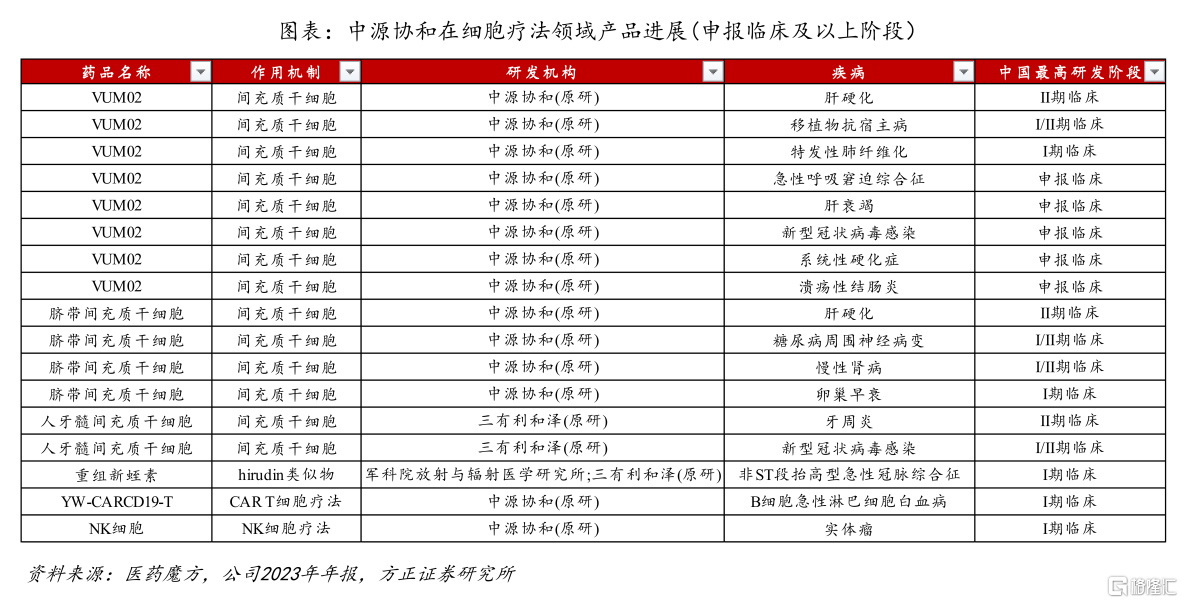
图片来源:方正证券研报
天士力也有入局,治疗慢性心力衰竭的人脐带间充质干细胞注射液正在开展I期临床;针对急性脑卒中6小时后急性期,布局的同种异体脂肪间充质基质细胞注射液,已获得FDA临床试验许可,并已在国内申报临床。
另外,九芝堂并购基金投资的北京美科也有多款管线:缺血耐受人同种异体骨髓间充质干细胞治疗缺血性脑卒中的Ⅱa期临床试验已完成31例受试者入组,治疗自身免疫性肺泡蛋白沉积症的“人骨髓间充质干细胞注射液”已完成8例受试者的入组。
已向港交所递交上市申请的泽辉生物,是中国首批获得PSC来源细胞疗法新药IND批准的公司、中国唯一一家目前有多项PSC来源细胞治疗资产处于II期临床试验的公司,拥有ZH901(已有4个适应证进入II期临床)、治疗帕金森病的ZH903、治疗干性年龄相关性黄斑变性(AMD)的ZH902等多个管线。
04
结语
干细胞疗法的革命性在于其“细胞再生”的核心机制——通过修复或替换受损组织实现疾病根源性治疗,而非仅缓解症状。这一颠覆性的治疗逻辑吸引着全球制药巨头纷纷布局。
与此同时,中国干细胞产业正乘着政策东风加速崛起,创新药物研发呈现爆发式增长,在数量上形成全球第二大研发梯队。
当政策、资本、临床形成创新合力,这片沃土必将孕育出改变医学史的“中国细胞”。
参考资料:
1.各家公司的财报、公告、官微
2.《20241222-中源协和-600645-立足“精准医疗”全产业链,抢滩干细胞创新药产业化发展空间》,方正证券
3.《20241222-医药生物行业:FDA首次批准干细胞疗法,国内新药亦蓬勃发展》,华福证券
4.国盛证券研报
 下载格隆汇APP
下载格隆汇APP
 下载诊股宝App
下载诊股宝App
 下载汇路演APP
下载汇路演APP

 社区
社区
 会员
会员




