近日,一则产业链上游的“知识产权纠纷”悄然引爆药企圈的神经。过滤膜国产代表企业科百特,与同行赛普涉RC除病毒膜技术的商业秘密侵权案终审宣判。浙江省高级人民法院作出了赛普停止销售现有RC除病毒膜包括改进品的判决。
表面上,这是一起涉及商业秘密的法律纠纷,实则暴露出生物医药产业中一个易被忽视却极具破坏力的环节——供应链稳定性,尤其在临床研发与药品注册过程中,一次看似细微的工艺或原材料变更,足以带来上亿元损失乃至产品上市延期。这场知识产权侵权风波的背后,隐藏着工艺生产过程中产品变更的结构性挑战,也对整个创新药生态提出了新的警示。
01 过滤膜之争背后,药品持续稳定生产安全隐患显现
事情还要追溯到2021年。
2021年3月,赛普公司在杭州成立。21年6月,赛普公司向国家知识产权局申请再生纤维素除病毒膜发明专利,技术方案为除病毒过滤膜的配方工艺;同时,同年8月,成立5个月其除病毒膜就通过了第三方验证,用当时的话来说,“仅数月便攻克卡脖子技术。”
不过,对于赛普技术的来源,科百特自2022年12月起,就赛普公司多款产品涉嫌存在知识产权侵权的行为发起了专利、技术秘密侵权诉讼,赛普公司及相关人员还卷入刑事案件。
科百特则是行业中的资深前辈,成立于2003年,20多年一直致力于各种微滤、超滤、除病毒过滤及中空纤维的研究、开发和制造。有意思的是,陷入纠纷的两家企业,均来自于杭州。而从后续的案件诉讼来看,两家公司商业纠纷的起因,是由多名从科百特离职的技术人员,跳槽到赛普公司所引发。
历时两年多,日前两家公司在RC除病毒领域的诉讼之争终于迎来终审判决,浙江省高级人民法院对科百特与赛普公司涉RC除病毒膜技术的商业秘密侵权案件作出终审判决。
无独有偶,生物技术巨头思拓凡诉国内企业百林科涉及一次性生物反应袋领域技术的专利侵权纠纷也同样在行业内引起广泛关注。如果这都仅是普通的知识产权纠纷案件,或许并不会引起产业如此广泛的反响。关键在于:过滤膜和反应袋都是药品生产中的关键“耗材”,处在至关重要的工艺节点——无菌过滤、纯化浓缩、生物反应产物分离等流程都离不开它,尤其在血液制品、抗体药、疫苗、细胞治疗等产品的生产中几乎不可或缺。
看到赛普相关产品被停售的判决结果后,有相关法律顾问认为,如果目前已有部分使用涉案产品的药企进入临床II期或III期阶段,因为禁售判决导致必须更换供应商,那么他们的生产工艺就需重新验证,并重新报批。除病毒膜和反应袋变更级别都较高,这对企业而言不仅是时间延误,更是不可预估的投入成本与市场窗口错失。
很多原料、设备、关键材料在药品注册时已经早早确定下来,变更难度极高。有长期关注药品供应链安全的业内人士告诉E药经理人,这场官司的结果影响的不仅仅是两家公司,更意味着,一个上游供应链的知识产权侵权纠纷,可能成为创新药商业化路径上的巨大绊脚石。
不少从事CMC(化学、生产与控制)管理的药企负责人表示,过滤膜与培养基、灌装瓶、一次性系统等工艺材料一样,属于注册资料中的“技术参数一部分”,变更流程复杂,且跨部门协调难度高。而现实中,很多新兴的生物药企在初期选择供应商时,往往更关注“交期与价格”,忽略了知识产权、企业经营稳定性、法规背景、验证历史这些看不见的“软指标”。这也是这场专利纠纷案背后,对行业更深层次的警示所在。
具体到过滤膜产业,其广泛应用于半导体、生物医药等领域,可以实现纳米级过滤,是所有过滤膜中技术含量最高的产品,2020年中国制药过滤产品市场销售额超过50亿元,到2026年预计年增长率超过15%。但长期以来,国内生物制药用除病毒滤膜产品市场被思拓凡(Cytiva)、默克密理博(Merck-Millipore)、旭化成(Asahi Kasei)等几家外国公司垄断,国产品牌市场渗透率极低。在新冠期间,由于全球供应链中断、进口产品涨价,迫使众多药企寻求国产替代。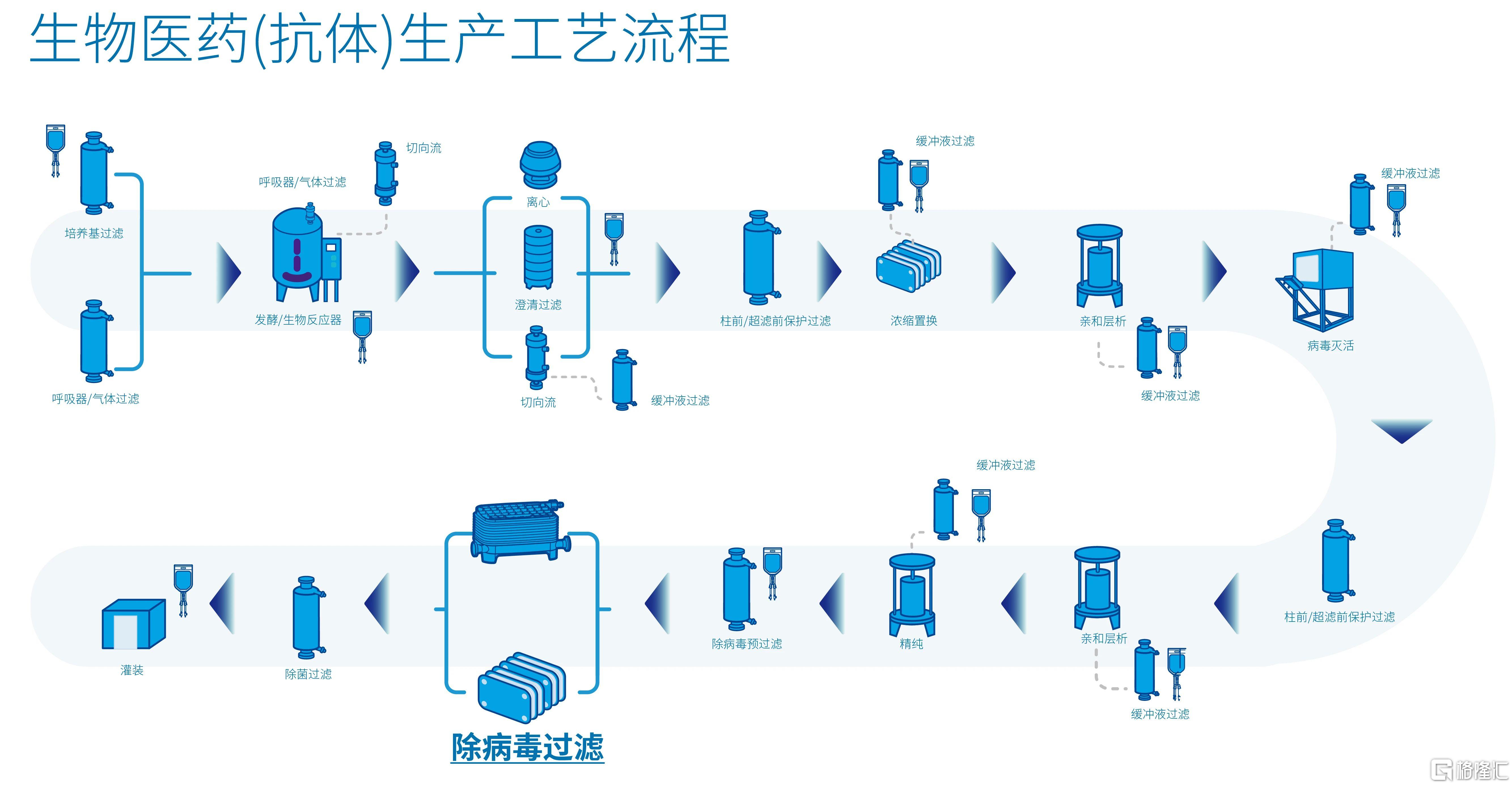
此后,国家发改委发布《产业结构调整指导目录》中明确指出鼓励突破包含膜分离材料的医药制品核心技术,进一步推动了一众本土企业的快速崛起。
据业内人士回忆,2020年前后,正值生物制品企业产能释放高峰,不少单位因缺膜停产。彼时,科百特已切入部分高端膜市场。科百特的兴起某种程度上是国产替代的缩影,它从半导体切入生物医药,完成膜材料的研发、验证、送样,成功与多个药企建立联合共建合作。然而正如一位投资人所说“做出膜不难,验证上药很难,稳定量产最难。”
“你永远不知道你所依赖的哪个部件和环节会在明天出事。”一位CMC从业者如此总结他对这件事的观感。事实上,“合法、安全、可替代”正成为当下药企选择供应商时的新三项基本原则。
02 卡脖子领域的突围与合规
除了过滤膜,中国生物药产业链中还有很多领域都正经历国产替代与合规挑战的双重考验,如培养基、填料等。
往远了说,自2020年的新冠疫情叠加贸易保护主义抬头,导致全球供应链面临严峻挑战,中国生物医药企业迫切需求实现产业链自主保障,为国内上游生物制药企业国产替代打开关键窗口期。色谱填料作为分离纯化技术的核心,在生物制药产业中处于关键地位。受益于中国生物药市场需求的加速释放,色谱填料的国产替代市场,正是在那时开启的。原为高壁垒领域是色谱填料,但目前已有如纳微科技等本土企业上市,形成相对充分竞争的局面。这一变化说明一旦国内厂商在验证能力、法规配套上形成闭环,是可以打破外资垄断的。
往近了看,今年初的中美贸易摩擦期间,外资企业原料价格飙升、交期不稳,倒逼国内培养基厂商加速替代。一位药企CMC负责人曾表示,你不能在进入NDA阶段时再发现培养基变更会影响细胞表达,那就是灾难,都可能影响你最终产品的上市节奏。
过去,药企在挑选供应商时重视的是价格、交付、客户服务,甚至“能否一起申报”这样的短期考量。如今,随着法规变化与合规理念升级,更多药企将供应商视作“产品质量的一部分”,甚至是监管合规链条的一环。
近年来,NMPA、FDA等监管机构均加强了对关键原料变更的审查——不仅要提供工艺比对、质量对比,还需提供详细的验证数据。这意味着,若原供应商发生法律问题导致材料无法继续使用,企业将陷入“补充试验-监管沟通-重新申报”的长期风险中。
因此,一个商业秘密纠纷官司,不仅会对药企形成直接波及,还可能间接引发产品注册资料缺陷、审批延期等风险。
前述法律顾问也给出了建议,药企在初期就应建立“供应商专利审查机制”,对合作方是否存在历史侵权纠纷、技术来源合法性进行尽调;此外,对关键材料供应商设置“合规+技术”双评估机制,按生命周期管理制度推进替代选项备案。
2025年,中国创新药进入深水区,BD交易频繁,IND与NDA密集递交,商业化路径加速。而创新药的未来,也注定是一场供应链的博弈:知识产权、原材料验证、跨境供应链依赖等,这些曾被忽视的“细枝末节”,正以更剧烈的方式影响着整个产业链的运行。
所以,中国药企必须在战略上重新认识“前端供应链”的价值——不只是“价格低”“交期快”,更是“可验证”“可备案”“能合规”。上游供应链管理同样是合规体系的一部分,创新成果才能真正快速落地。
国产替代大势已至。科百特和赛普之间的纠纷,作为国产技术崛起中的一个插曲,提醒整个行业:防患于未起时,才能保证真正的可持续。
相关信息来源:
1.科百特与赛普RC除病毒膜商业秘密侵权案件进展
https://mp.weixin.qq.com/s/4RqjcooASZcqX98ADofAUg
 下载格隆汇APP
下载格隆汇APP
 下载诊股宝App
下载诊股宝App
 下载汇路演APP
下载汇路演APP

 社区
社区
 会员
会员




